アインシュタインの光電効果をがん細胞の中で再現 放射線治療への新展開(プレスリリース)
- 公開日
- 2021年07月14日
- BL14B1(QST 極限量子ダイナミクスII)
2021年7月14日
京都大学アイセムス(物質-細胞統合システム拠点)
・がん細胞内で電子を発生してDNA を効率よく切断する方法を開発
・新規の放射線治療※1)の開発に向けた前進
京都大学アイセムスの玉野井冬彦教授らの研究グループは、がん細胞内にヨウ素※2)元素を含むナノ粒子を取り込ませ、これにX 線を当てることで、がん細胞のDNA を切断し、細胞死を誘導できることを明らかにしました。また、X 線のエネルギーを調整することで、DNA切断の効率を高められることを明らかにしました。 金属原子に光を当てることで電子を放出させる現象は、アインシュタインの光電効果※3)と呼ばれています(図1)。この現象の解析により、アインシュタインは光が粒子と波の両方の性格があることを1905年に提唱しました。さらに彼の書いた論文が、その後の量子物理学の基礎を作ったと考えられています。本研究成果は、まさに、アインシュタインの光電効果を、がん細胞内で再現する試みです。 また、従来の放射線治療では、X線が細胞内の主に水分子をイオン化して活性酸素を発生させることでDNA切断を引き起こす、いわば間接効果が多いのに対し、本研究では、DNAのすぐ近傍でヨウ素にX線を当てることで電子を発生させてDNA切断を引き起こすという直接効果を得ることに成功しました。直接効果を促進することにより、放射線治療の効率を大きく上げられると考えています。 本成果は、英国時間7月14日午前10時(日本時間 午後6時)に、英科学誌「Scientific Reports(サイエンティフィック・リポーツ)」にオンライン掲載される予定です。また、本研究は、量子科学技術研究開発機構、カリフォルニア大学アーバイン校と共同で行いました。 論文タイトル・著者 |
背景
放射線治療はがん治療の重要な柱として広く使われています。X線などの放射線をがん細胞にあてると、細胞内の分子のイオン化を引き起こすことで、DNAを切断し、がん細胞を殺すことができます。直接DNAに作用することもありますが、実際には、X線の大部分は細胞内の70%を占める水に作用し、その結果発生する活性酸素が二次的にDNAを切断するという間接的な作用によりがん細胞にダメージを与えます。そのため、特に低酸素状態であるがんの中心部では活性酸素ができにくく、治療の効率が悪くなるという課題がありました。
これまで本研究グループは、多孔性シリカというナノ粒子※4)を用いた研究に取り組んできました。ナノ粒子というのは直径30~400ナノメートル(1ナノメートルは1ミリメートルの100万分の1)の微粒子のことです。このナノ粒子はがん細胞に効率よく取り込まれ、細胞核の近くに留まります。また、がんのかたまり全体に万遍なく散らばります。さらにナノ粒子はがんに蓄積する能力をもっています。今回、多孔性シリカにヨウ素を含ませ、がん細胞に送り込むことを目指し研究を進めました。
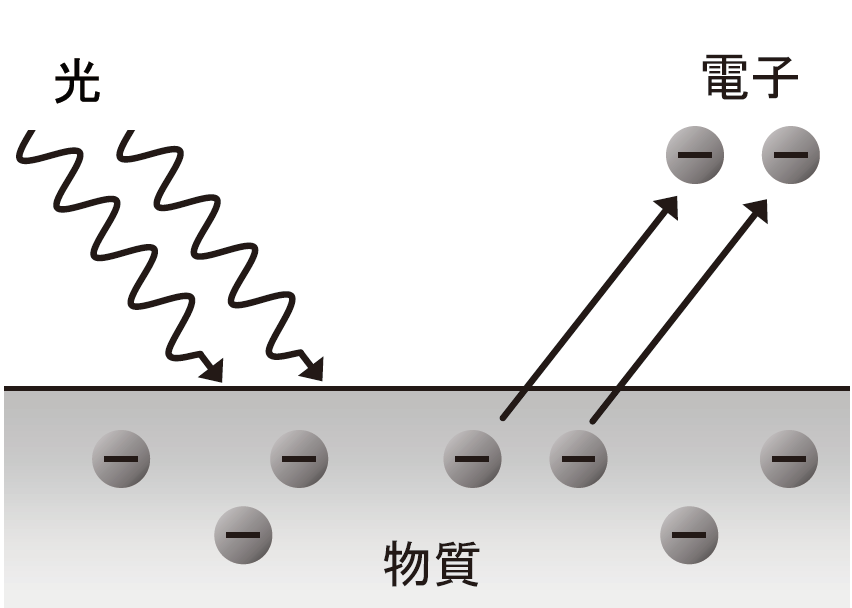
一方で、研究グループは、アインシュタインが提唱した光電効果に注目しました。光電効果とは、金属原子などの物質に光をあてた時に電子が放出されるという現象です。アインシュタインはこの現象を解析し、光が粒子と波の両方の性格をもつことを提唱しました。1905年に彼が書いた論文が、その後の量子物理学の発展に大きく貢献したと考えられています。
光電効果が起きると原子内で連鎖反応が起き多数の電子が放出されることが知られています。原子核の一番近くのK殻にある電子がX線のエネルギーによりたたき出されるとその空隙を埋めるために外側の殻にある電子がK殻に落ちてきます。その時に放出されたエネルギーを受け取った電子がさらに放出されます。
(こうして出てきた電子は「オージェ電子」と呼ばれています。)すなわち光電効果は、多量の電子の放出を可能にする現象です。私たちは今回このアインシュタインの光電効果をがん細胞の中で再現し、がんの中心部に対しても効率的な放射線治療法の開発に向けた研究を進めることにしました。
図1.光電効果
研究内容と成果
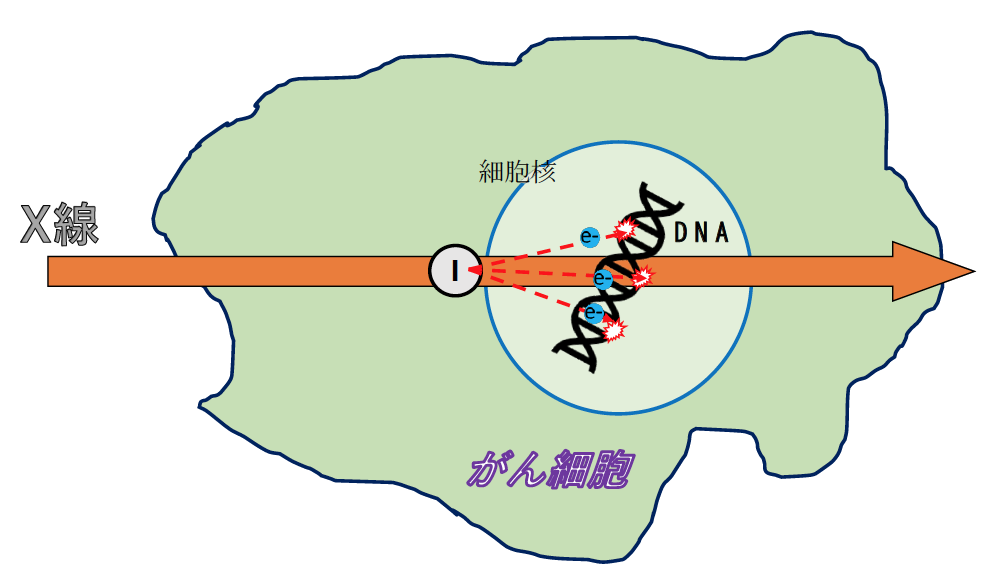
研究グループは、まずヨウ素を含み生体内で分解される安全性の高い多孔性シリカのナノ粒子を合成しました。こうしてできたナノ粒子はがん細胞に効率よく取り込まれがん細胞の核の近傍にヨウ素を運ぶことができます。この時、がん細胞にX線をあてると光電効果によりヨウ素から電子がたたき出され、細胞核にあるDNAの切断をひきおこします(図2)。
今回の研究では、三次元のがん細胞のかたまりであるがんスフェロイドを用いて、上に述べたアイデアが実現されることを証明しました。がんスフェロイドにヨウ素を含むナノ粒子をまんべんなく分布させてからX線を照射すると、ヨウ素を含んだナノシリカが存在する状況下では照射時間依存的にがんスフェロイドを破壊することができました。
解析の結果、ヨウ素が含まれるナノ粒子の存在下で、X線を照射することによりDNAの二重鎖切断が起きていること、またその結果として細胞死(アポトーシス)が起きていることが確認できました。
図2.光電効果をがん細胞の中で引き起こす試み
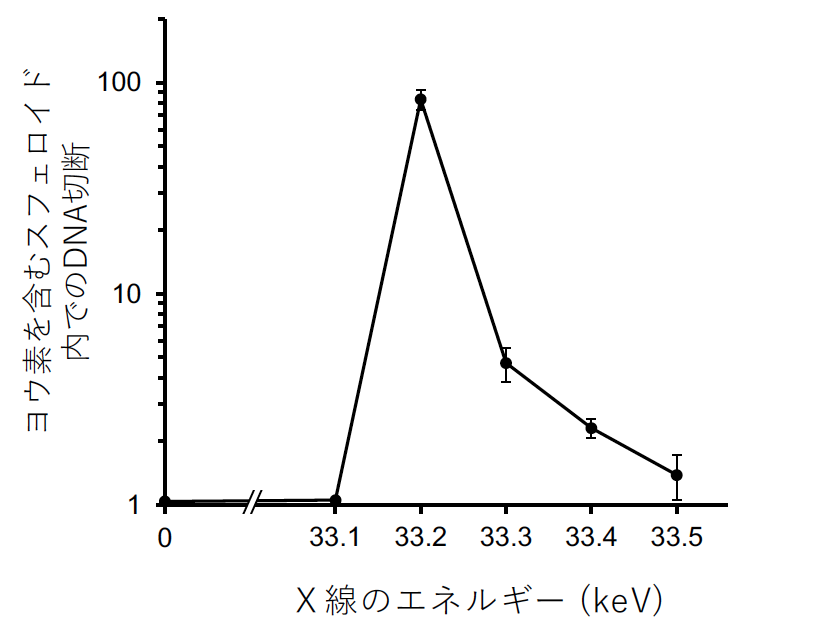
興味深いことに、図3にあるように、X線のエネルギーを33.1 keVから始めて33.2, 33.3, 33.4, 33.5 keV と増やしてDNA二重鎖切断への影響を見た結果、33.2 keVで明確なピークが見られることが明らかになりました。この結果は最適効果をもたらすためのX線のエネルギーを調節できることを示しています。
ヨウ素原子にX線をあてたときに電子が放出されるのは、X線を構成する光子(光量子)のエネルギーをヨウ素の電子が受け取りその電子が放出されることによるものです。電子が放出されるためには、一定の強さのエネルギーをもったX線を照射する必要があり、それぞれの元素でその値が決まっています。ヨウ素の場合は33.2 keVであり、この値を超えると電子が放出されることになります。一方で、放出された電子のエネルギーが高すぎると飛距離が大きくなり、その効果がさがってしまいます。すなわち、最適な電子の放出を調節する必要があり、今回の実験でこれが可能なことが示されました。
図3.最適効果を引き起こすX線エネルギー
今後の展開
今後、放射線増感剤としてヨウ素を含むナノ粒子が用いられることで、放射線治療の効率が上がることが期待されます。また、ヨウ素はCTスキャンなどの診断のために用いられており、本研究にて開発した材料が、広くがん治療、診断に役立つ可能性があります。さらに、私たちのアプローチではDNAの近くで電子を発生させDNA切断を引き起こすので、DNAへの直接効果が期待され、がんの中心部のような低酸素条件下でも使うことが可能です。今後、私たちの開発した手法は、新規の放射線治療の開発に役立つと考えられます。
研究プロジェクトについて
科研費: JSPS KAKENHI Grant No. JP20H00331
補足説明
※1 放射線治療:
がん治療の一つで広く使われている。放射線をがん細胞にあてて殺す。
※2 ヨウ素:
元素の一つで、健康サプリとしてヨード塩やヨード卵など、広く使われている。また放射線の甲状腺への影響を軽減することなどに使われている。日本は世界有数のヨウ素資源大国であり、特に千葉県は世界中で利用されているヨウ素の約4分の1を生産している。日本の埋蔵量は世界一、経済的に回収できるヨウ素のうち75%以上を保有していると言われており、ヨウ素可採年数は600-700年と言われています。
※3 光電効果:
物質(Matter)に光をあてると電子の放出がみられる現象のこと。
※4 ナノ粒子:
30-400 nmサイズの微粒子。
(SPring-8 / SACLAに関すること) |
- 現在の記事
- アインシュタインの光電効果をがん細胞の中で再現 放射線治療への新展開(プレスリリース)