Topic 24 ナノ細孔材料へのガス分子吸着現象の解明
ガスを旺盛に吸着する多孔性配位高分子の秘密を探る
活性炭が脱臭や水質浄化に活用されるのは、その表面に多数の微細な穴(細孔)をもち、有機物などを吸着するからだ。こうした細孔をもつ物質はナノ細孔材料と総称される。中でも近年注目を集めるのが金属イオンと有機分子によって合成される多孔性配位高分子である。多孔性配位高分子は、水素をはじめ、多様なガスを高密度で吸蔵でき、しかもさまざまな機能をデザインできるという長所をもっている。多孔性配位高分子のナノ細孔がガスを吸着するメカニズムは、世界に先駆けてSPring-8で次々と解明されている。その快挙を水素吸蔵合金に関する研究成果とともに紹介しよう。
意図した機能をもつナノ細孔材料をデザインする
2002年2月、北川進教授率いる京都大学グループは、名古屋大学の高田昌樹助教授(現・理化学研究所主任研究員)、大阪大学の小林達夫教授、名古屋大学の坂田誠教授(現・名誉教授)らと共同で、開発済みだったナノ細孔材料に酸素を整然と吸着させる研究を開始した。このナノ細孔材料は、銅やコバルトなどの金属イオンと有機分子が結合した多孔性配位高分子で、室温で多様な気体を吸蔵できる。しかも数gでバスケットボールコートからサッカーグラウンドまでの表面積をもつのだ。「ナノ細孔材料によって気体を自在に集積できることを示したかったのです」と北川教授は目的を語る。
実験に使われたのは、0.4×0.6 nm(ナノメートル=10-9 m)の細孔をもち、酸素を吸着するCPL-1という銅配位高分子である。試料粉末をマイナス183℃に冷却し、粉末結晶構造解析ビームラインBL02B2 で放射光回折を行うと、酸素分子の吸着による回折パターンが観測された。獲得したデータを名大グループの考案した情報処理法で解析したところ、細孔には固体に近い凝集状態で整然と酸素分子が並んでいることが確認された。また酸素分子は細孔方向と平行に2列に並ぶはしご構造をとり、最も近接した分子間距離は約0.32 nmであることも判明した(図1)。こうした多くの新事実は2002年12月に米科学雑誌『Science』に紹介された。
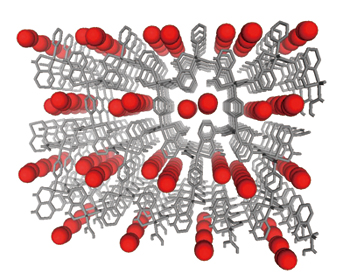
CPL-1のつくる細孔に酸素分子(赤い球で示されている)が規則正しく並んでいる。
燃料電池で期待される高い水素吸蔵能
合成が容易で自在にデザインできる多孔性配位高分子に水素が吸蔵できれば、燃料電池にも活用できる。2003年4月、北川進教授は、大阪女子大学の久保田佳基講師(現・大阪府立大学准教授)、JASRIの高田昌樹主席研究員(現・理化学研究所主任研究員)らと共同で、先に酸素吸着実験でも用いたCPL-1に水素を細孔内に吸着させ、その水素分子の直接観測を試みた。一般に電子が1個しかない水素原子をX線で観測することは至難とされてきた。「ナノ細孔材料の合成を進めるために水素分子の振る舞いを知る必要があったのです」と北川教授。
試料は、高い角度分解能をもつ粉末結晶構造解析ビームラインBL02B2に持ち込まれ、粉末X線回折実験が実施されたが、ここで得たデータも十分ではなかった。そこで高田主席研究員らは、希少なデータから電子密度を解析する新たな技術を開発した。
こうしてディスプレイに映し出された電子密度分布図(図2)は、多孔性配位高分子の銅原子に結合した酸素原子の近くに水素分子が存在することを示した。しかも細孔壁面には凹凸があり、水素分子はくぼみにはまるように存在し、出入りが容易な状態だった。細孔と分子のサイズが合えば理想的な貯蔵法になることが確認されたのだ。この成果は独化学会誌『Angewandte Chemie(応用化学)』国際版に掲載され、ナノ細孔材料のイメージが表紙を飾った。
一方、水素貯蔵材料としてもっとも期待されるのは水素吸蔵合金である。2001年5月、豊田中央研究所の則竹達夫主任研究員、坂田誠名古屋大学名誉教授らは、水素化マグネシウムMgH2という水素貯蔵合金の電子密度分布の解析を試みた。当時の水素吸蔵合金の水素貯蔵量は2重量%程度であり、軽量で水素密度の高い合金の開発が求められていた。マグネシウムは、7.6重量%という水素貯蔵能をもち、軽量だ。ただしMgH2は300℃以上に加熱しないと水素は放出されない欠点をもっている。「これを克服するには基礎に立ち返り、MgH2で結合を担う電子の分布を調べる必要があったのです」と則竹主任研究員は当時を振り返る。
MgH2粉末をBL02B2に持ち込み、高輝度X線を当てると水素の電子密度分布がしだいに明らかになっていく(図3)。
ここで注目すべきなのは電子数だ。MgH2のマグネシウム領域は半径0.09 nmの球状で、電子数は1.91個少ない陽イオン、水素領域は半径0.1 nmの球状で電子が0.26個多い陰イオンになっていた。つまり両者はイオン結合をしているのだ。また結晶内全体に拡がる電子密度は非常に低く、金属結合は存在せず、マグネシウムと水素の電子が重なり合う共有結合がわずかに存在することも判明した。「水素を吸蔵すると水素原子は自由電子を引きつけて陰イオンとなり、マグネシウムは水素とイオン結合し安定な状態になるのです」と則竹主任研究員。研究成果は、2002年9月、学術論文誌『Applied Physics Letters』に掲載された。
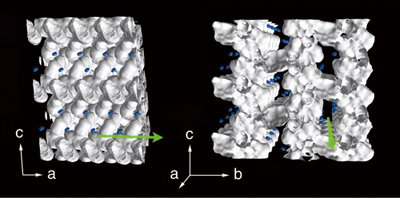
青い粒が水素。水素分子は細孔の中央ではなく、少し細孔壁に寄った位置に、しかし、配位高分子とは独立して規則的に配列していることがわかる。
Yoshiki Kubota, Masaki Takata, Ryotaro Matsuda, Ryo Kitaura, Susumu Kitagawa, Kenichi Kato, Makoto Sakata, Tatsuo C. Kobayashi: Direct Observation of Hydrogen Molecules Adsorbed onto a Microporous Coordination Polymer; Angewandte Chemie International Edition; 2004, Vol. 44, page 922. Copyright Wiley-VCH Verlag GmbH & Co. KGaA. Reproduced with permission.
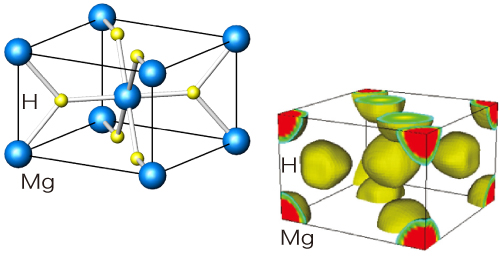
MgH2の結晶構造(ルチル型構造)と電子密度ρ=0.3e/(0.1 nm)3で囲まれる面を描いた。マグネシウムは陽イオン、水素は陰イオンになり、イオン結合をしている。
アセチレンガスの吸蔵状態を解明
2006年、京都大学の北川進教授のグループは、ナノ細孔材料がアセチレンを吸着する過程の観測をBL02B2を使って試みた。
アセチレンはナノ細孔と非常に強い相互作用をもち、細孔内に高密度で納まる一方で、吸着過程はいくつかの状態変化をともなうことが北川グループの2005年のBL02B2での研究によって明らかにされ、英科学誌『Nature』に報告されていた。「反応性の高いガスの吸着材料として多孔性配位高分子を活用するためには、ガス分子導入以降の状態をさらに解明する必要がありました」と北川教授は語る。
研究グループはBL02B2において、まず銅配位高分子粉末をガラスキャピラリ(極細ガラス管)に充填し、そこにアセチレンガスを導入した。圧力と温度を制御しながら、粉末回折データを測定。この際、すべての回折データを同時に二次元検出器で測定できるカメラ半径287 mmの大型デバイシェラーカメラが活用された。
その結果、アセチレン分子は、飽和状態では細孔壁の酸素原子と水素結合し、高密度で吸着していることがわかった。また中間状態から飽和状態への構造変化は小さく、アセチレン分子と細孔壁との結合は飽和状態よりかなり弱いこともわかった(図4)。そして吸着後、結晶格子は中間状態でいったん膨張し、その後、細孔の方向にスライドして変形し、飽和状態に達して収縮しており、アセチレン分子の形状と細孔壁との相互作用によって柔軟に構造を変化させながら取り込まれることが明らかになった。この成果は2006年7月『Angewandte Chemie』国際版に掲載された。
ナノ細孔材料は、天然ガスの低圧安定吸蔵や温暖化ガスの吸着、有害物質の分離などへの応用、さらに超伝導材料や磁性材料開発の可能性も高く、今後の成果が予測される。
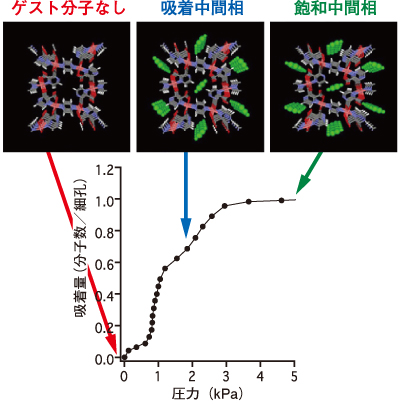
ナノ細孔の方向から見たもので、緑色で描いた分子がアセチレン分子。アセチレン分子とその両側の酸素原子との間に化学結合はほとんど見られない。
- 目次に戻る
- 次のページ
Topic 25 電池材料の研究 - 前のページ
環境 ・ エネルギー /人類生存の礎をミクロに解明する