アメフラシ体内物質の制がん効果を追って
海洋生物アメフラシとは
海辺に生きる軟体動物アメフラシを知っていますか。貝類と同じ仲間に属しながら、背中に負っているはずの貝殻がすっかり退化してしまったアメフラシは、茶色っぽい紫色をした長さ15cmほどの生物です。浅瀬に住んで海藻を食べるので、磯の潮溜まりをゆっくり移動する姿にときどきお目にかかります。
こんな名前がついたのは、雨が降っているときに磯辺によく集まるからとも、体を刺激すると紫色の体液を出して雨雲のような煙幕をはるからとも言われます。いずれにしても、美しくもなく食用にするわけでもない、あまり目立たない生き物なのですが、意外にもアメフラシは科学者たちの関心を集めてきました。
その理由のひとつは、神経について研究する科学者たちが、アメフラシの巨大神経細胞(といっても直径1mmほどですが)を実験の材料として愛用してきたため。そしてもうひとつは、制がん剤になりそうな物質がアメフラシの体内から見つかっているからです。今回紹介するのはこの制がん剤候補物質についてのホットな研究成果です。
アメフラシ由来の制がん剤候補物質がどんな構造をもち、どんなしくみでがん細胞を働かなくするのか、その謎に挑んでいるのが(独)理化学研究所播磨研究所に所属する平田邦生研究員(当時(財)高輝度光化学研究センター協力研究員)や(財)高輝度光化学研究センター利用研究促進部門高田昌樹部門長たちです。謎解きは大型放射光施設SPring-8を利用して行われています。
制がん剤候補はこんな構造
自然界の物質からがんに効く薬を見つけだそうという研究は昔からさかんに行われてきました。天然物から見つかって、がん治療に使われている薬は多数あります。たとえばマイトマイシンCは微生物から、ビンブラスチンはツルニチニチソウという植物から見つかりました。
海洋生物から制がん剤を見つけようという研究もさかんです。アメフラシから「アプリロニンA」という物質をはじめて見つけ出し、これに強い制がん作用があることを最初に確認したのは、名古屋大学山田靜之名誉教授でした。
山田名誉教授は三重の海岸に生息するアメフラシを何十kbも採ってきてそれをすりつぶし、微量のアプリロニンAを取り出しました。がん細胞を仕込んだネズミにこの物質を与えると、与えないネズミに比べて長く生きることを実験で確かめたのです。アプリロニンAはがん細胞に働いて、その働きを抑える力をもっていることが明らかになりました。今ではその制がん効果は、強力な制がん剤として使われているマイトマイシンCを上回ることがわかっています。
山田名誉教授のお弟子さんだった筑波大学木越英夫教授は化学の専門家で、 NMR(核磁気共鳴)という方法を用いてこの物質の立体的な構造を明らかにし、またこの物質の合成にも成功しています。
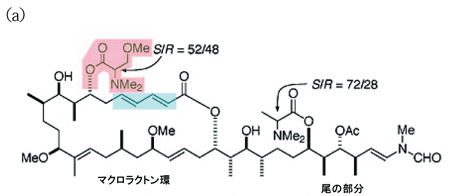
アプリロニンAの構造を図で見てみましょう(図1)。マクロラクトン環とよばれる炭素の骨格をもった大きな環状構造に複雑に折れ曲がった尾がついている様子が見て取れます。それでは、いったいどの部分が制がん作用を発揮するのでしょうか。逆に言えばこの物質はがん細胞にとってなぜ毒として働くのでしょう。
山田名誉教授のグループはこの研究によって、アプリロニンAが生体内のアクチンに働くことを解明しました。アクチンはタンパク質の一種で、真核生物が細胞内に一番多くもっているタンパク質です。細胞膜の内側に網目状に広がって細胞の形をつくり、また細胞の運動を司る基本的なタンパク質として知られています。
アクチンは多数の分子が重合*してフィラメント状になったり、またひとつずつの分子(単量体)に戻ったりしていますが、アプリロニンAがアクチンに取り付くと、バラバラの単量体のままになって、フィラメントには戻らなくなることが判明しました。アクチンの働きにとっては致命的な事態です。細胞骨格が保てず細胞が破綻してしまいます。
図1.左半分は主にマクロラクトン環で、右半分は主に炭素鎖で構成されている尾の部分。
図中、ピンク色でトリメチルセリンを、水色でジエンを取り囲んでいる。原子間を結ぶ線が太い部分は紙面から手前側、点線部分は紙面より向こう側に結合が出ていることを表現している(立体配置)。S/Rは矢印で示した炭素原子を中心に正四面体構造が反転(立体配置が反転する)している状態を比率で示している。 Meはメチル基(CH3)を示している。
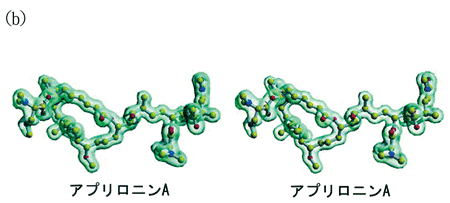
★左図と右図を立体視(平行法)してご覧下さい。
(a)の構造式に対応させてみると構造がよくわかる。黄:炭素 赤:酸素 青:窒素
結合体をSPring-8で解析
さて、このあたりからいよいよ平田研究員たちの登場です。平田研究員はタンパク質の構造を調べる専門家です。学生時代からSPring-8にやってきて、様々なタンパク質の構造解析に取り組んできました。
X線でタンパク質の構造を調べるにはタンパク質を結晶にしておかなくてはなりません。アクチンの場合、結晶にするには重合体(フィラメント)では不可能です。しかし、アクチンは通常なら重合してフィラメント状になってしまうので、単量体のまま調べるという条件がなかなか整いません。ところが、アプリロニンAはアクチンと結合するとアクチンを単量体に分解し、それぞれの単量体と1対1で結びつくので、結合体のままうまく結晶にすることができます。平田研究員は「無色透明の六角柱の結晶がすぐにできました」とうれしそうに話します。 150×100×50ミクロンという小さい柱状結晶でした。
さらに、朝できたアクチン-アプリロニンA結合体の良質な結晶は、その日のうちにタンパク質構造解析用のビームラインBL38B1で測定し、 0.145ナノメーターという高い解像度で構造解析を行うことができたのです。すでにわかっていたアクチンの構造を差し引くかたちで、アプリロニンAの構造が判明しました。また、どんな具合にアクチンと結合しているのかも見えてきました(図2)。
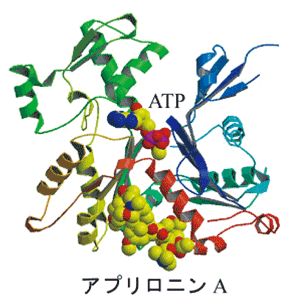
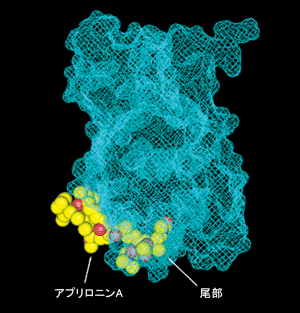
図2.
(a).アクチン-アプリロニンA複合体構造の全体図
アクチンはリボン図、アプリロニンAとATP(アデノシン三リン酸)はCPKモデル(球体のモデル)で表示してある(黄色:炭素、赤:酸素、青:窒素)。アプリロニンAは疎水的なアミノ酸で構成されている「疎水性クレフト(溝)」に結合していることがわかった。アクチン自体には大きな構造変化は無かった。
(b).(a)図から90度回転させて横から見た図(回転軸は上下方向)
アクチンは水色のアミ目で表されており、アプリロニンAが尾を差し込んで結合している様子が見える。
脱重合*作用と制がん作用
アプリロニンAとアクチンはどのように結合しているのでしょうか。アプリロニンAが環状部分と尾から成り立っていることは先に述べました。結合体の構造解析から見えてきたのは次のような事実です。
アクチンが重合してフィラメント状になるときにアクチン分子どうしが結合する部分として知られている溝に、アプリロニンAは尾を差し込む形で結合しています。このためアプリロニンAに邪魔されてアクチンどうしが重合できなくなると考えられます。
このことは、以前に木越教授のグループがアプリロニンAの尾の部分を取り除いた構造の分子を合成し、この化合物ではアクチンをフィラメント状に重合させない(脱重合)効果が失われていることを確認していた事実とぴったり符合します。
一方、フィラメント状のアクチンを単量体に脱重合する化合物がすべてがん細胞に対する毒性を発揮するわけではないこともわかってきました。これは制がん活性に必要な特性ではありますが、それだけでは十分ではないのです。
平田研究員たちは、最近、細胞のアポトーシス(自発的な死)と脱重合の関係に注目するようになりました。アクチンのフィラメントを脱重合させる物質をがん細胞に加えると、この細胞にアポトーシスが起こることが報告されているからです。
また、アプリロニンAの環状の部分から突き出したトリメチルセリンと呼ばれる部分(図1(a)のピンクの部分)が、がん細胞に対して毒性を発揮することが知られています。「この部分がアポトーシスの信号になっているのかもしれません」と、平田研究員は制がん活性のメカニズムについて考えを巡らせています。
「まだ、決定的なことはわかりません。さらに生化学の専門家のサポートもほしいところです」と平田研究員。がん細胞を壊す新しいメカニズムの解明と、興味ある制がん剤が生まれる可能性をもつこの研究が、これからどんな展開を見せるのか、大いに注目したいものです。
取材・文:サイテック・コミュニケーションズ
用語解説
●重合・脱重合
重合とは簡単な構造をもつ分子化合物が二つ以上結合して高分子を生成する。この際に結合された化合物が重合体(ポリマー)と呼ばれ、元の分子化合物は単量体(モノマー)と呼ばれる。
脱重合とは重合体から単量体に分解していく反応。
この記事は、(独)理化学研究所播磨研究所 放射光科学総合研究センター 研究技術開発室 平田邦生氏(成果発表当時、(財)高輝度光科学研究センター 協力研究員)にインタビューをして構成しました。