簡便な手法により、化学の常識を覆す鉄酸化物を発見 - 安価な新磁石、酸素材料、超伝導体開発へつながるか -(プレスリリース)
- 公開日
- 2007年12月13日
- BL02B2(粉末結晶構造解析)
平成19年12月13日
国立大学法人 京都大学
フランス国 レンヌ第一大学
フランス国 ラウエランジュバン研究所
財団法人 高輝度光科学研究センター
|
京都大学、高輝度光科学研究センター、仏・レンヌ大学、ラウエランジュバン研究所は共同で、低温での簡便な化学反応により、組成が単純で新しい構造をもつ鉄酸化物を合成することに成功しました。(小手先の新しさではなく)その根源的な新しさが評価されて、英国科学誌「Nature」誌(12月13日電子版)に論文が掲載されることになりました。 (論文) |
1. 研究の背景
資源・元素の安定確保が緊急の課題といわれる世界状況の中で、新種の鉄酸化物の開拓と新機能の発掘は重要性を増しています。鉄は地球上に広くそして多量に存在するユビキタス元素ですので(酸素、ケイ素、アルミニウムに次ぐ4番目)、入手しやすく安価であり、また生体にとって安全な元素だからです。酸素も勿論同様です。鉄の酸化物は多彩な機能をもっており、安価な磁石、カードやテープ用の磁気記録材料、あるいは顔料(ラスコーの壁画の赤色やコピー機の黒色トナー、化粧品)などとして広く使われてきました。ところで、一見多種多様にみえる鉄酸化物もミクロな構造(鉄原子とそれを取り巻く酸素原子の結合形態)には多くの共通点を有しており、それを制御して新たな機能をもつ鉄酸化物を開拓するのは困難と考えられていました。
2. 研究成果の内容
京都大学のグループは、最近、高温でおこなう通常の合成に低温でおこなう合成を組み合わせることにより、鉄酸化物の構造を局所的に制御する簡単な合成法を開発しました。今回、合成に成功した鉄酸化物はSrFeO2(Sr: ストロンチウム、 Fe: 鉄、 O:酸素)です(図1)。これまで一般に鉄酸化物の鉄原子のまわりの酸素原子は、四面体、八面体、ピラミッドのような立体的な結合形態をとると考えられていました。しかし、この新しい鉄酸化物では、鉄原子のまわりに四つの酸素原子が正方形状に配位し(平面四配位と呼ばれます)、さらにその正方形が互いに繋がり合って二次元面を作っていることが、第三世代の大型放射光施設(SPring-8)の粉末結晶構造解析ビームラインBL02B2で測定した粉末回折データ(図2)を解析することにより明らかになりました。これは、鉄酸化物に関する膨大な研究に基づくこれまでの無機化学の常識を覆すものであり、これからの基礎学術と応用の展開に大きな可能性を感じさせるものです。
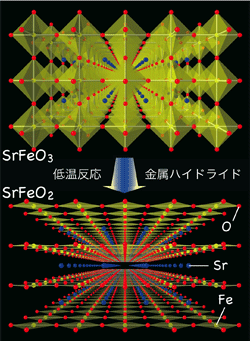 図1.SrFeO3(上)の低温反応により、平面四配位構造をもつSrFeO2(下)が得られました。黄、赤、青丸はそれぞれFe、 O、 Sr原子を表します。
図1.SrFeO3(上)の低温反応により、平面四配位構造をもつSrFeO2(下)が得られました。黄、赤、青丸はそれぞれFe、 O、 Sr原子を表します。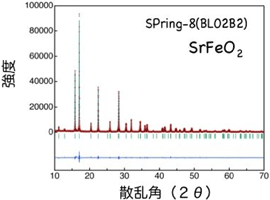 図2.SPring-8で測定した放射光X線回折データ。リートベルト解析によって無限層構造が決定されました。
図2.SPring-8で測定した放射光X線回折データ。リートベルト解析によって無限層構造が決定されました。具体的には、良く知られたペロブスカイト構造*1の鉄酸化物SrFeO3から基本構造を壊さないまま大量の酸素(全体の三分の一)を規則的に取り除き、新物質SrFeO2を得ることに成功しました。このように酸素を奪う反応のことを還元反応といいます。鉄酸化物に限らず金属酸化物から酸素を奪う(還元する)には、各種ガスを用いたり、電気化学を用いたりするのが一般的でしたが、本研究で用いたのは金属ハイドライド(CaH2;Ca:カルシウム、H:水素)です。金属ハイドライドは、有機化学では溶媒の蒸留の際に脱水剤として日常的に使われる安価な試薬です。これを金属酸化物の低温での還元反応のための試薬として最初に用いたのは英国の無機化学のグループですが、それほど注目されてはいませんでした。一方、京都大学のグループでは、エネルギー消費量が少なく、しかも(構造の部分変換に基づく)新物質開発に有効な低温合成により、新しい磁性材料開発を4年前から進めてきました。鉄酸化物に対して金属ハイドライドによる低温反応を行うアイディアはこれまでの研究の流れから自然にうまれたものです。
SrFeO2の合成の秘訣は、金属ハイドライドの強力な還元作用とともに、この反応が金属酸化物の通常の合成温度(約1000℃)に比べ低い温度(300℃)で行われたことにあると考えられます。出発物質の原料と混合し、ガラス管に封入、最後に加熱するだけの極めて簡便で安価なプロセスです。
鉄の平面四配位のように珍しい配位状態が、SrFeO2のような単純な組成のイオン結合性*2物質から得られたことは、(すでに膨大な量の研究の蓄積がある化学の歴史を鑑みて)化学の教科書の基礎(の基礎)を書き換える画期的な出来事です。また、複雑化する一方の現代科学にも新しい視点と夢を与えます。珍しい配位状態を得るために、従来は、有機分子を金属のまわりに位置させるなど、手法、得られる物質ともに複雑化していく傾向にありました。複雑化すると、単にコストがかかるだけでなく、例えば、機能と無関係の無駄な体積が増える(効率の低下)、金属と金属の距離が広がる(相互作用の低下)などの問題が生じていました。金属ハイドライドを使う手法は、単純な組成の他の鉄酸化物(あるいは遷移金属酸化物全般)から珍しい配位状態を得る、簡便で画期的な手法として今後発展していくことが期待できます。
3. 今後の展開
どんな複雑な酸化物でも、その機能の根幹は、金属のまわりの酸素の結合形態(配位状態)によります。珍しい配位状態をもつSrFeO2は機能性としても以下に示すような大きな可能性を秘めています。
1 超伝導:SrFeO2は高温超伝導銅酸化物の中で最も単純な構造で“無限層”構造*3として知られている物質SrCuO2(Cu:銅)と全く同一の構造です。鉄酸化物では画期的といえる平面四配位も、銅酸化物ではありふれた状態です。今回得られたSrFeO2は絶縁体ですが、元素置換などによって電子や正孔(ホール)を注入することができれば、鉄酸化物で初の(高温)超伝導を実現できる可能性があります。
2 酸素材料:SrFeO2の合成の出発物質として用いたSrFeO3は、その構造の中に酸素欠陥を作ることができるため、「SrFeO3 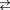 SrFeO2.5 + 0.25O2」の反応を利用した酸素イオン伝導材料(固体燃料電池)、酸素センサー、酸素分離膜、触媒などの安価な酸素材料の研究が世界中で熾烈に行われています(図3)。本研究によって、酸素変化量が「SrFeO3
SrFeO2.5 + 0.25O2」の反応を利用した酸素イオン伝導材料(固体燃料電池)、酸素センサー、酸素分離膜、触媒などの安価な酸素材料の研究が世界中で熾烈に行われています(図3)。本研究によって、酸素変化量が「SrFeO3 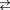 SrFeO2+ 0.5O2」と2倍になったことで、こうした酸素材料の効率化、小型化が期待できます。さらに、この反応が約130℃と極めて低温から開始することから(図4)、従来、高温領域のみで有効(電子と違い酸素は重く、大きいことから固体中では高温にしないと動けない(反応しない)ためです)であった酸素材料の低温動作化につながると期待できます。
SrFeO2+ 0.5O2」と2倍になったことで、こうした酸素材料の効率化、小型化が期待できます。さらに、この反応が約130℃と極めて低温から開始することから(図4)、従来、高温領域のみで有効(電子と違い酸素は重く、大きいことから固体中では高温にしないと動けない(反応しない)ためです)であった酸素材料の低温動作化につながると期待できます。
3 強力磁石: メスバウアー分光、中性子回折実験より、SrFeO2の磁気的な相互作用は、同じ価数をもつ既存の鉄の化合物の中で最強であることがわかりました。これは鉄が平面四配位をとる効果であると考えられます。SrFeO2では隣り合う電子スピンが反対向きに並ぶ(反強磁性秩序*4といわれます)ため、磁石として使うことはできませんが、本研究の金属ハイドライドを使った低温合成を他の鉄酸化物(例えば、既存の鉄酸化物磁石)に応用すれば、これまでにない強力磁石を開発できる可能性があります。
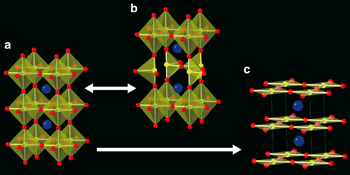 図3.(a)SrFeO3、(b)SrFeO2.5、(c) SrFeO2の構造。黄、赤、青丸はそれぞれFe、O、Sr。本手法により、(a)から(c)への構造変換に成功。従来は(a)と(b)の間で数多くの研究が展開されていました。
図3.(a)SrFeO3、(b)SrFeO2.5、(c) SrFeO2の構造。黄、赤、青丸はそれぞれFe、O、Sr。本手法により、(a)から(c)への構造変換に成功。従来は(a)と(b)の間で数多くの研究が展開されていました。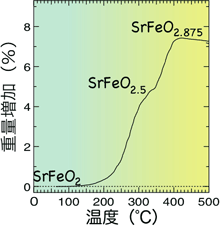 図4.SrFeO2の酸素1気圧中での酸素吸収過程。130℃もの低温から酸素の吸収を始めます。
図4.SrFeO2の酸素1気圧中での酸素吸収過程。130℃もの低温から酸素の吸収を始めます。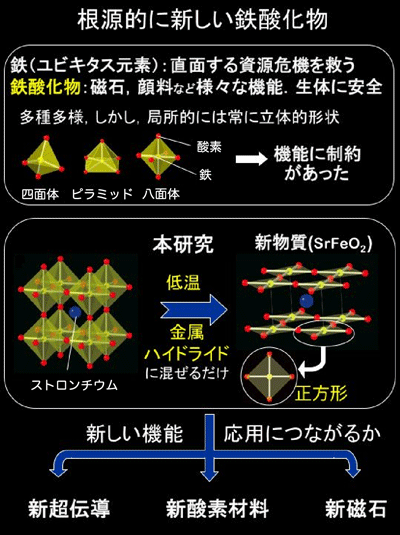 本研究の概念図
本研究の概念図<用語解説>
*1 ペロブスカイト構造
一般式AMO3と表される無機物の代表的構造です。Aにはアルカリ金属、アルカリ土類金属、希土類金属が、Mには遷移金属が入ります。
*2 イオン結合性
陽イオンと陰イオンの電気的な力に基づく化学結合性。塩(NaCl)はイオン結合性物質の代表例ですが、金属酸化物のほとんどがイオン結合性をもつとみなせます。
*3 無限層構造
数多く発見されている高温超伝導銅酸化物は例外なく、銅と酸素からなる2次元面(CuO2面)と、超伝導に無関係のバッファ層の繰り返しで構成されています。高温超伝導体の構造を分類するときに、バッファ層に挟まれたCuO2面の枚数により、一層、二層、三層 …と呼ばれます。バッファ層がない(最も単純な)ケースでは、CuO2面は“無限”層あるとみなせます。SrFeO2は、無限層構造SrCuO2と同一構造です。
*4 反強磁性秩序
結晶中で隣合う遷移金属上の電子スピンが反対向きに並ぶ状態を反強磁性秩序といいます。上向きと下向きの磁気モーメントが打ち消し合いますので、全体としては磁気モーメントをもちません。磁石として使われる強磁性秩序は磁気モーメントの向きが全て揃います。
|
<問い合わせ先> (研究内容に関すること) (ビームラインに関すること) (SPring-8全般に関すること) |
- 現在の記事
- 簡便な手法により、化学の常識を覆す鉄酸化物を発見 - 安価な新磁石、酸素材料、超伝導体開発へつながるか -(プレスリリース)